CH4是主要的温室气体及重要的化工原料[1-2],因此,CH4转化具有重要的意义。由于CH4稳定的化学结构使其很难被高效转化[3],低温等离子体技术可以打破热力学平衡的制约,在温和条件下,实现CH4的非平衡直接转化[4]。介质阻挡放电(DBD)作为常用的低温等离子体的产生方式,因设备简单、放电稳定、反应条件温和,被广泛应用[5]。单纯DBD放电转化CH4存在产物选择性低的问题,将DBD放电技术与催化剂相结合是改善该问题的有效方法[6]。
Sungkwon等[7]通过Al2O3和Pt/Al2O3的对比实验研究了催化剂电导率对CH4转化的影响,评估了等离子体和导电催化剂之间的协同作用。Zhu等[8]指出等离子体与Ni/γ-Al2O3催化剂协同作用可促进CH4转化。Mahammadunnisa等[9]通过添加CuO/CeO2、NiO/CeO2和Cu-Ni(5-5)/CeO2催化剂到DBD放电反应器,可提高甲醇的选择性。近年来,过渡金属氧化物CeO2被广泛应用于CH4转化。研究结果表明,CeO2晶体表面富有氧空位,具有适宜的供氧能力,因此利于催化CH4部分氧化生成合成气[10-11]。徐锋等[12]在Cu-Zn-Al/HC-AE 催化剂中添加助剂 Ce,单位能耗CH4转化量提高了9.75%,单位能耗CH3OH产量提高了76.6%。众多学者对等离子体与催化剂协同转化CH4进行了研究,笔者基于CeO2-CuO-ZnO/γ-Al2O3催化剂辅助等离子体转化CH4的实验及催化剂的BET、SEM和XPS表征,分析催化剂中的CuO与ZnO物质的量比和CeO2对催化剂性能的影响。
1 实 验1.1 实验装置及方法催化剂辅助等离子体转化CH4的实验装置如文献[13]所示。不同的是本研究DBD反应器介质阻挡材料为刚玉管。在前期实验研究的基础上,确定文中的实验基础条件为:输入电压75 V、放电频率10.42 kHz、总流速218 mL/min、甲烷流量79 mL/min、水蒸气流量31 mL/min、O2/N2物质的量比0.53、催化剂添加量1 g、反应时间20 min、催化剂床层温度200 ℃。
在实验时,将石英棉支撑的催化剂填装于反应器中,进行催化剂辅助等离子体转化CH4的实验。生成的CH3OH经蒸馏水冷凝吸收后,用 GC9790 型气相色谱仪检测、GDX-102 型填充柱、FID 检测器以及外标法进行计算。不凝气用 GC9790Ⅱ型气相色谱仪检测、TDX-01 型填充柱、FID 检测器以及外标法计算。
1.2 转化率与产率的计算根据反应前后气体总流量与CH4反应前的体积分数计算CH4转化率、碳氧化物及烃类产物(CO、CO2和C2烃)产率、H2产率、CH3OH产率。
CH4转化率为
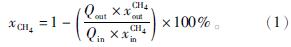
碳氧化物及烃类产物产率为
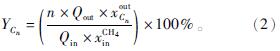 )
)
H2产率为
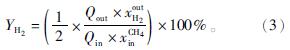
CH3OH产率为
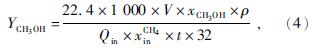
式中:Qin——反应前气体总流量,mL/min;
Qout——反应后气体总流量,mL/min;
xCH4in——反应前气相中CH4体积百分数,%;
xCH4out——反应后气相中CH4体积百分数,%;
xoutH2——反应后产物H2的体积百分数,%;
xoutCn——反应后产物CO、CO2和C2烃的体积百分数,n=1,2,%;
xCH3OH——液体样品中CH3OH的体积百分数,%;
V——甲醇吸收液(蒸馏水)的体积,mL;
ρ——甲醇密度,g/cm3;
t——反应时间,min。
1.3 催化剂制备与表征1.3.1 催化剂制备(1)CuO-ZnO/γ-Al2O3
用70 ℃温水溶解定量的Zn(NO3)2(分析纯,天津市致远化学试剂有限公司)、Cu(NO3)2(分析纯,天津市致远化学试剂有限公司)和K2CO3(分析纯,天津市致远化学试剂有限公司),并与一定量的γ-Al2O3(分析纯,天津市科密欧化学试剂有限公司)混合,磁力搅拌下制得溶胶。将所制的溶胶移入水浴恒温锅中,在70 ℃下水浴加热100 min,使溶胶变为凝胶。凝胶自然冷却后,于104 ℃干燥箱中干燥4 h,得到的固结物经研磨、400 ℃空气焙烧3 h,制得系列CuO-ZnO/γ-Al2O3(m:n)催化剂,其中,m:n为CuO与ZnO物质的量比。
(2)CeO2-CuO-ZnO/γ-Al2O3
将制得的CuO-ZnO/γ-Al2O3凝胶(m:n=1:1)冷却,室温下加入按CeO2质量分数5%计量的Ce(NO3)3(分析纯,天津市致远化学试剂有限公司)溶液,放置12 h,去除上层清液,于80 ℃条件下水浴5 h后,先后经104 ℃干燥 2 h、400 ℃条件下空气焙烧3 h,制得目标催化剂,记为5% CeO2-CuO-ZnO/γ-Al2O3(1:1)。
1.3.2 催化剂表征采用BELSORP-miniⅡ型物理化学吸附仪和JSM-5600LV型扫描电镜进行BET和SEM表征,通过ESCALAB型光电子能谱仪进行XPS表征,实现催化剂表征。
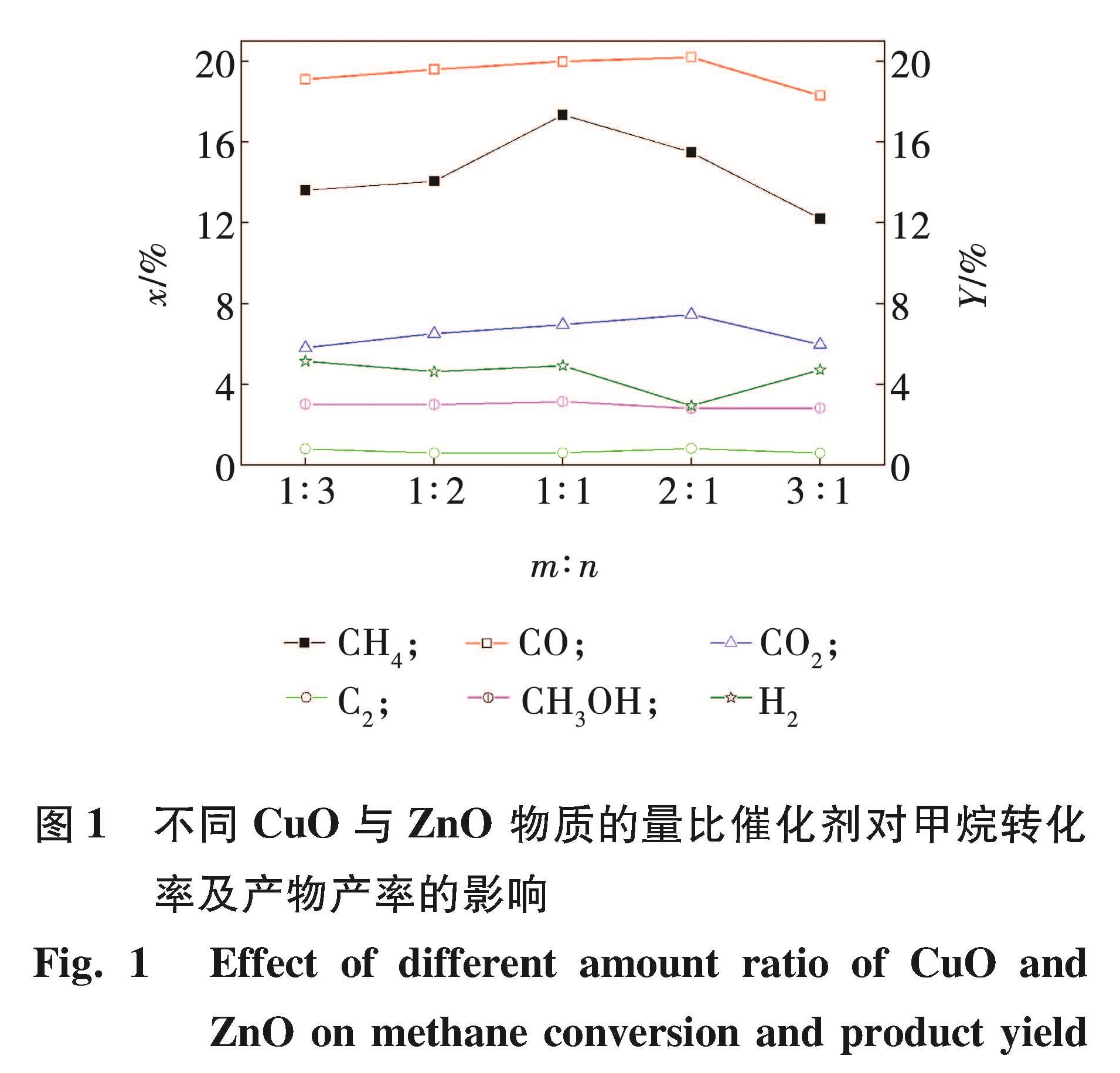
2 结果与讨论2.1 反应性能2.1.1 CuO与ZnO物质的量比的影响将CuO/ZnO物质的量比m:n为1:3、1:2、1:1、2:1和3:1的CuO-ZnO/γ-Al2O3催化剂,分别填装于DBD反应器中,进行催化剂辅助等离子体转化CH4的实验,考察CuO与ZnO物质的量比对反应性能的影响,如图1所示。
图1 不同CuO与ZnO 物质的量比催化剂对甲烷转化率及产物产率的影响
Fig.1 Effect of different amount ratio of CuO and ZnO on methane conversion and product yield
从图1可以看出,该反应的主要产物为CO、CO2、CH3OH、H2及C2H4、C2H6等C2烃,而CH4转化率及除H2外的其它产物产率伴随CuO与ZnO物质的量比的增大变化规律为先增后降。这可能是由于不同CuO与ZnO物质的量比致使CuO和ZnO在催化剂表面富集的程度不同而导致的。
该反应等离子体段的主要作用是改变催化剂段的进气组成,为催化反应提供更多的活性基团及易反应的中间产物。Magureanu等[14]采用与本研究相同结构的反应器进行等离子体-催化处理,气相VOCs的实验表明,放电区域产生的O3等稳定性物质在催化剂表面吸附、分解,产生氧化性更强的单氧活性基团,大大促进了污染物的降解。
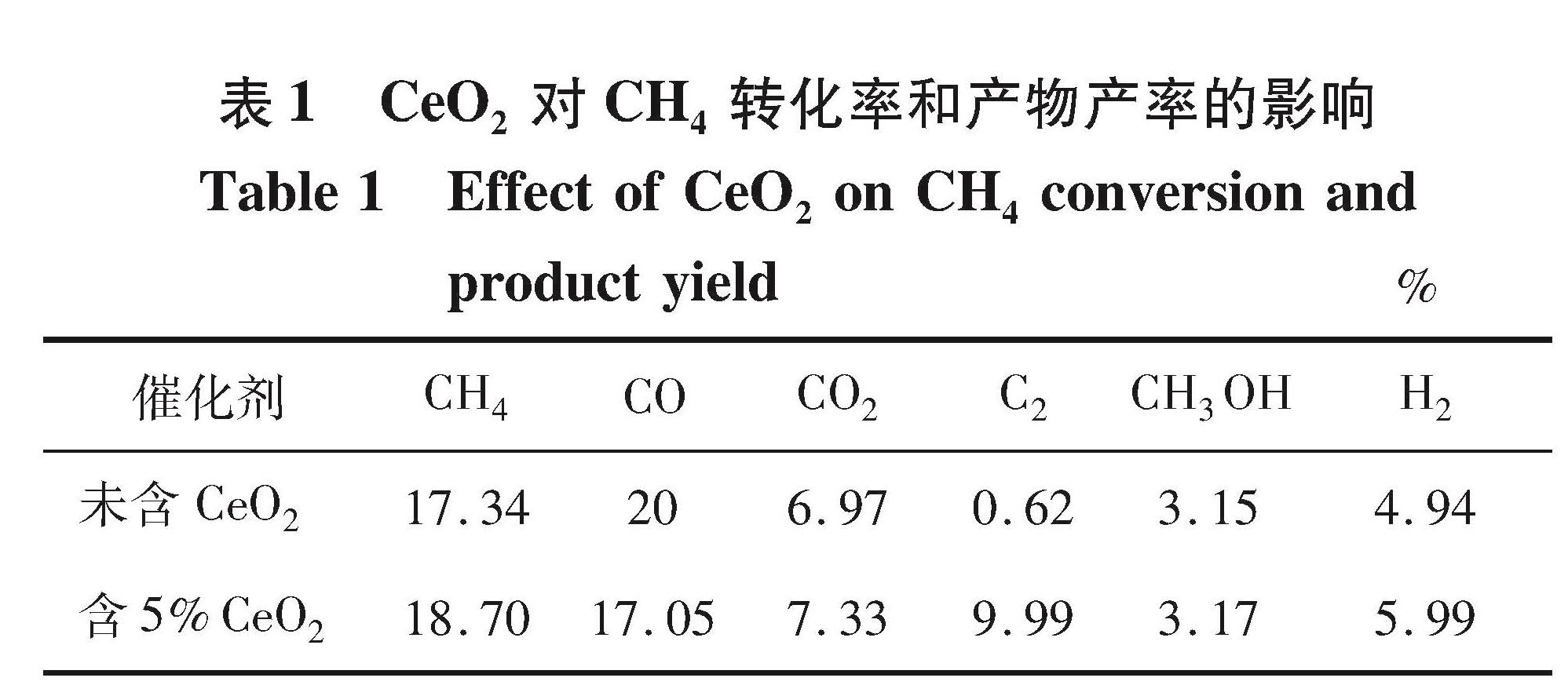
2.1.2 CeO2的影响由图1可见,当CuO与ZnO物质的量比为1:1时,CH4转化率和CH3OH产率取得最大值,分别为17.34%和3.15%。当CuO与ZnO物质的量比为2:1时,CO、CO2及C2产率最高,但此时的CO产率(20.2%)与CuO与ZnO物质的量比为1:1时CO产率(20%)相差无几,且H2产率(4.94%)仅次于最高值5.16%,因此,以CuO与ZnO物质的量比为1:1的CuO-ZnO/γ-Al2O3为基础催化剂制备5% CeO2-CuO-ZnO/γ-Al2O3,并将其填装于DBD反应器中,进行催化剂辅助等离子体转化CH4的实验,考察CeO2对反应性能的影响,如表1所示。催化剂中添加 CeO2利于CH4转化和H2生成,对CH3OH的生成基本无改进效果,但可显著促进 C2烃的生成。CeO2可以通过Ce4+和Ce3+之间的转换,在CeO2晶格中容易形成氧空位[15]。氧空位可与吸附于催化剂表面的氧分子反应生成活性很强的表面氧物种O-2和O-,促进表面氧化反应[16-19],对于甲烷转化反应而言,更宜将CH4氧化为烃类等碳氢化合物[20]。
表1 CeO2对CH4转化率和产物产率的影响
Table 1 Effect of CeO2 on CH4 conversion and product yield%
2.2 催化剂的结构特征2.2.1 比表面积和孔结构
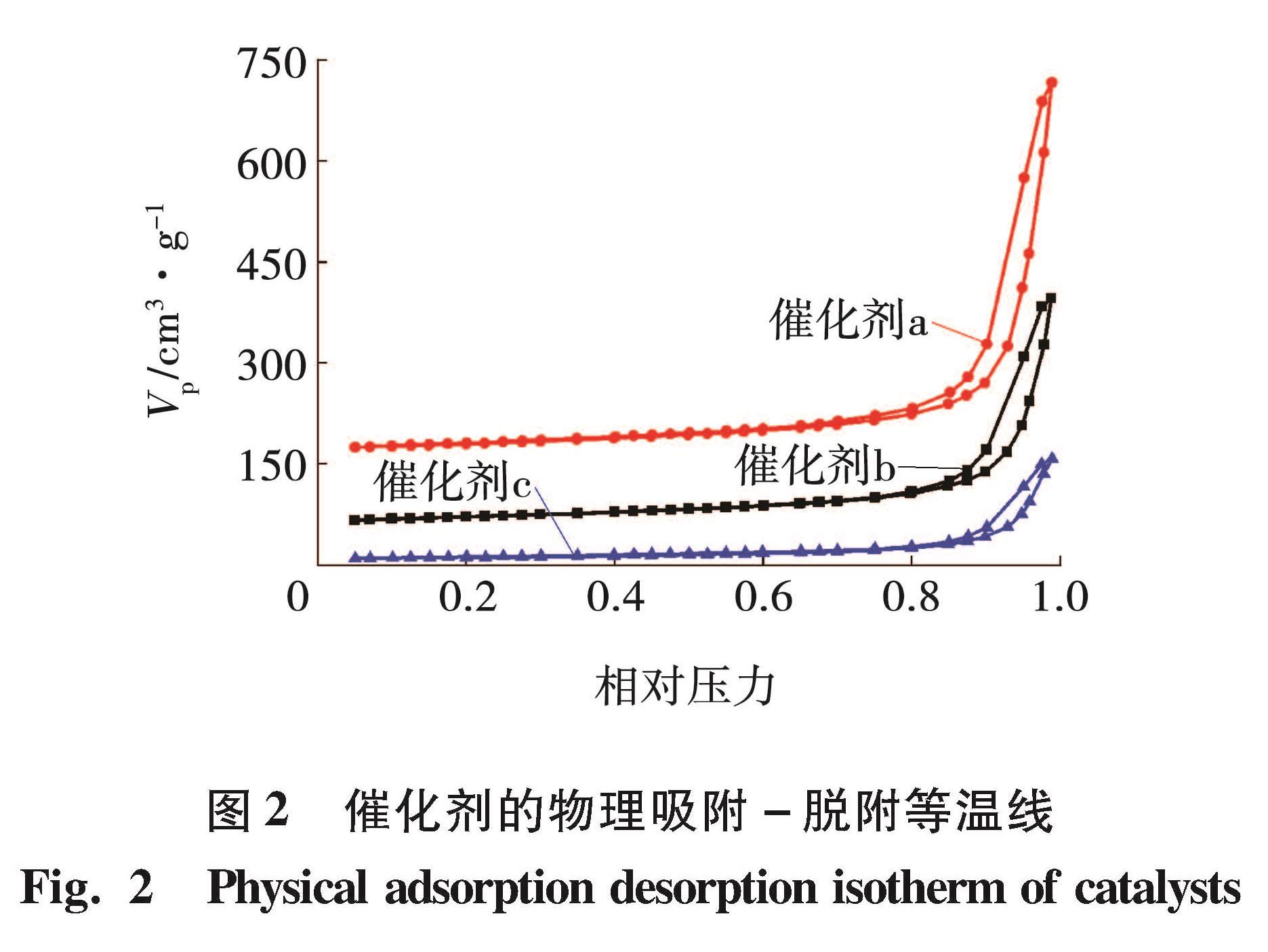
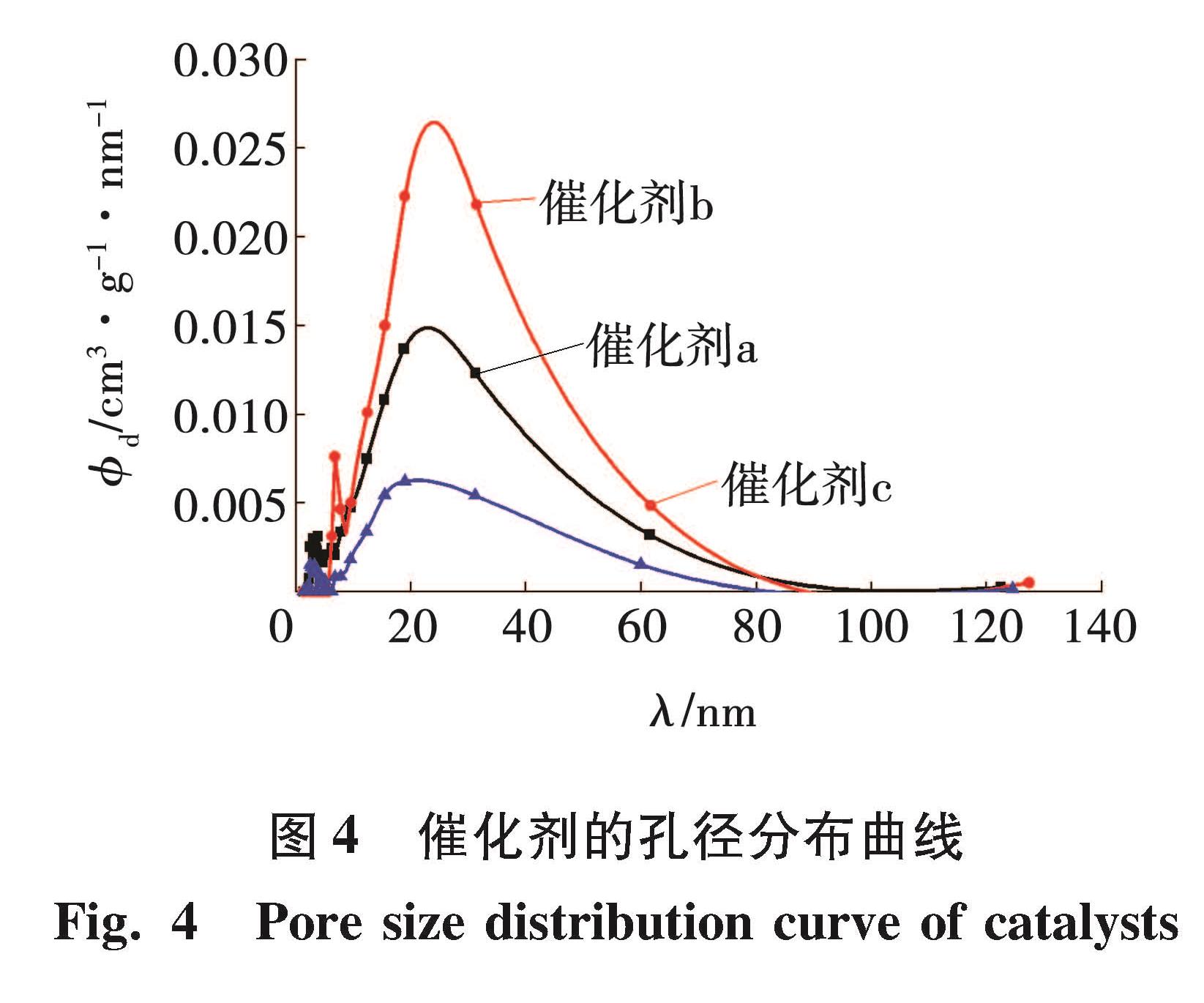
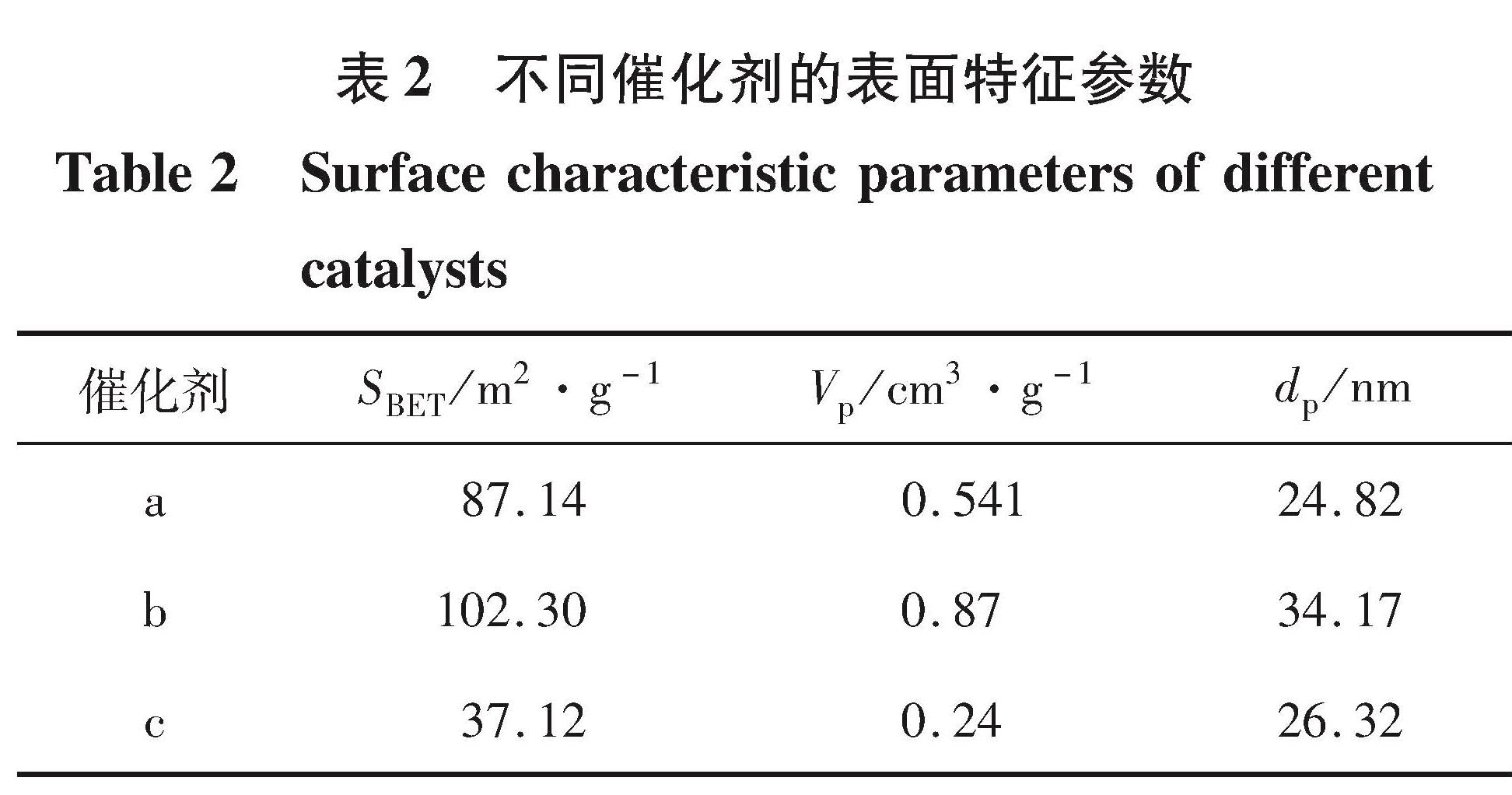
对m:n分别为1:1和2:1两种CuO-ZnO/γ-Al2O3催化剂记为催化剂a和催化剂b,以及5% CeO2-CuO-ZnO/γ-Al2O3(1:1)催化剂c进行了BET和SEM表征,如图2所示。不同催化剂的SEM谱图如图3所示。催化剂的孔径分布φd曲线如图4所示。由图2可见,三条等温曲线均属于IV型吸附曲线,具有毛细管凝聚现象,说明催化剂存在孔结构。三条等温曲线均存在回滞环,且低压区吸附脱附重合比较好,说明催化剂存在微孔; 回滞环起点在相对压力0.8以后,说明催化剂有大孔结构; H3型回滞环,说明存在介孔结构,且为形状不规则的堆积孔,与图3所示的SEM表征结果相吻合。
图4和表2分别给出了三种催化剂的孔径分布曲线及对应的孔结构参数。由图4和表2可知,CuO与ZnO物质的量比以及CeO2对催化剂的表面特征参数具有较大的影响。提高CuO与ZnO物质的量比,有助于改善催化剂的介孔结构和比表面积,这可从图4显示的CuO-ZnO/γ-Al2O3(2:1)比CuO-ZnO/γ-Al2O3(1:1)介孔数量多得以证实。催化剂中添加CeO2,在焙烧过程中可能因孔壁坍塌,部分小介孔变成大介孔,而小部分介孔转变为大孔,致使催化剂比表面积和孔容减小,而平均孔径变大。CH4部分氧化属于温和的放热反应,且反应基本上发生在催化剂表面。催化剂比表面积和孔容减小,不利于反应气及中间产物的扩散,也不利于反应热的及时传递。也就是说,随着催化剂比表面积和孔容减小,催化剂的活性会降低,不利于CH4转化和产物生成。但图1和表1所示的反应性能与此恰相反,这可能是在实验基础条件一定的情况下,CH4部分氧化反应不仅受催化剂比表面积和孔结构的影响,更受活性组分在载体表面分布的影响。
2.2.2 表面物种
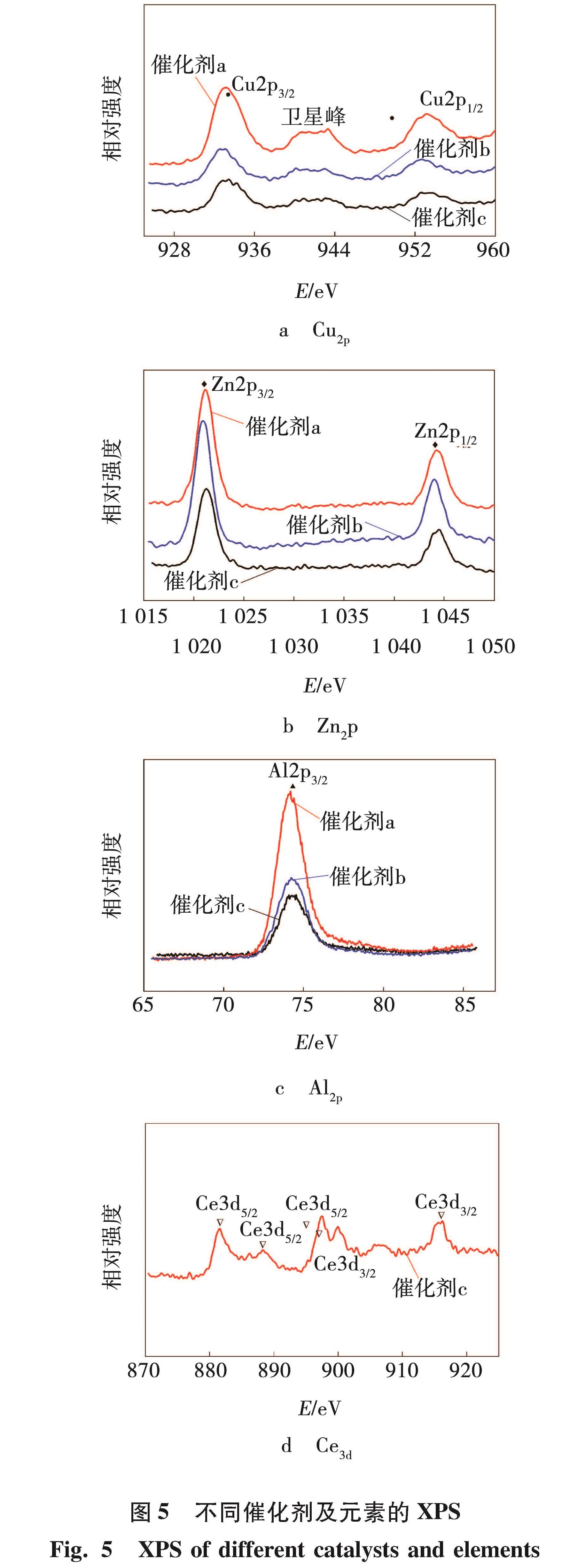
图5是CuO-ZnO/γ-Al2O3催化剂m:n分别为1:1和2:1,以及5% CeO2-CuO-ZnO/γ-Al2O3(1:1)的XPS表征结果如图5所示。由图5 a可以看出,结合能933 eV处存在,其归属于Cu2p3/2,而结合能为953 eV附近的峰归属于Cu2p1/2,结合能为943 eV附近出现卫星峰,与标准图谱进行对比知,催化剂中的Cu为CuO结构。由图5 b 可以看出,在结合能1 021 eV附近出现Zn2p3/2特征峰,此时Zn为ZnO结构,添加CeO2后,Zn2p3/2特征峰向高结合能方向移动是表面Zn元素化学环境变化所致; 在结合能1 045 eV处出现Zn2p1/2特征峰,此时Zn为ZnAl2O4结构。由图5 c可以看出, Al2p3/2特征峰存在于结合能74 eV处,此时Al为Al2O3结构。由图5 d可以看出,在结合能882、888、898 eV处存在Ce3d5/2特征峰,而在结合能900 和916 eV处存在Ce3d3/2特征峰。由此知,5%CeO2-CuO-ZnO/γ-Al2O3(1:1)催化剂中的Ce为CeO2结构。
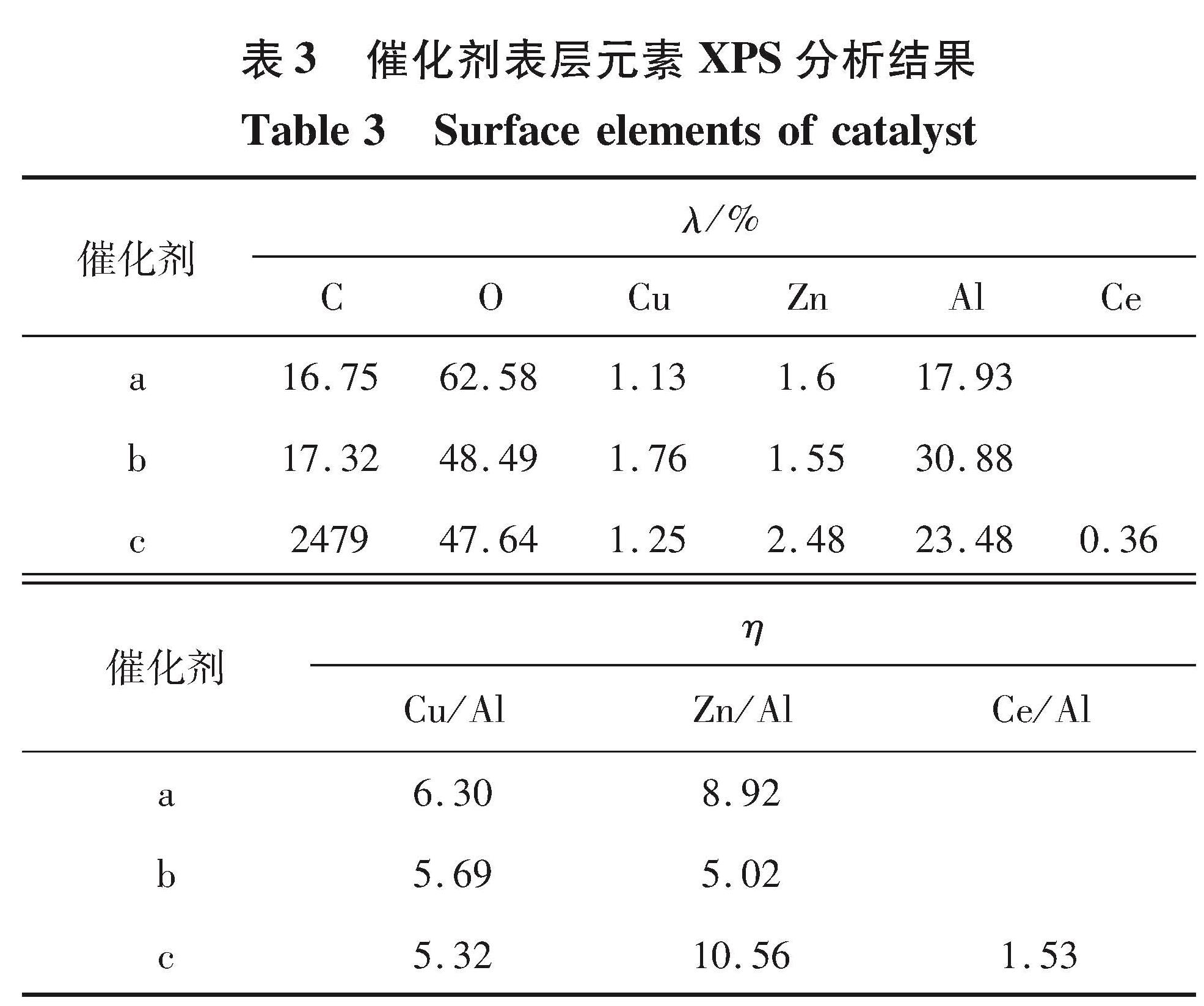
催化剂表层元素XPS分析结果如表3所示。在CuO-ZnO/γ-Al2O3 及CeO2-CuO-ZnO/γ-Al2O3中,Cu/Al值、Zn/Al值及Ce/Al值可近似表示催化剂表面的金属分散性。由表3可知,CuO-ZnO/γ-Al2O3(1:1)的Cu/Al值和Zn/Al值η均高于CuO-ZnO/γ-Al2O3(2:1),即CuO-ZnO/γ-Al2O3(1:1)表面活性组分的分散性较高。这是CuO-ZnO/γ-Al2O3(1:1)的催化活性高于CuO-ZnO/γ-Al2O3(2:1)的原因,且与2.2.1节的分析结果相一致。
对比添加CeO2前后催化剂表层元素的分析结果可知,Cu在5%CeO2-CuO-ZnO/γ-Al2O3(1:1)表面富集程度不如CuO-ZnO/γ-Al2O3(1:1),而Zn在5%CeO2-CuO-ZnO/γ-Al2O3(1:1)表面的富集程度明显增强。结合表1所示的催化剂辅助等离子体转化CH4的实验结果,推测5%CeO2-CuO-ZnO/γ-Al2O3(1:1)表面的Cu对CH3OH生成起主要催化作用,而Zn对H2和C2烃的生成催化作用更显著。
3 结 论
(1)CeO2-CuO-ZnO/γ-Al2O3辅助等离子体转化CH4的主要产物为CO、CO2、CH3OH、H2及C2H4、C2H6等C2烃。
(2)催化剂中的CuO与ZnO物质的量比对CH4转化率及主要产物产率均有影响,文中CuO与ZnO物质的量比为1:1较合适。催化剂中CeO2利于CH4转化和H2生成,可显著促进 C2烃的生成,但对CH3OH的生成基本无改进效果。
(3)在实验基础条件一定的情况下,CH4部分氧化反应不仅受催化剂比表面积和孔结构的影响,更受活性组分在载体表面的分布影响。催化剂中添加CeO2对改善载体表面Zn活性组分的分散性具有重要促进作用。
- [1] 徐 锋, 聂欣雨, 李 凡, 等. 甲烷和水蒸气介质阻挡放电转化的影响因素[J]. 黑龙江科技大学学报, 2020, 30(1): 56-60.
- [2] 杨 娟, 陈鹏宇, 戴 俊,等.CO3O4/WO3复合催化剂的合成及可见光催化转化甲烷制甲醇[J]. 燃料化学学报, 2022, 50(4): 464-473.
- [3] 张百明, 张 航, 岳晨阳,等. 金属有机框架催化甲烷直接转化研究进展[J]. 中国科学: 化学, 2021, 51(2): 165-174.
- [4] 徐 锋, 李 创, 朱丽华. 低温等离子体促进煤层甲烷活化转化[J]. 黑龙江科技大学学报, 2015, 25(6): 597-601.
- [5] 李 凡, 朱丽华, 徐 锋. 介质阻挡放电等离子体甲烷/水蒸气重整制氢[J]. 燃料化学学报, 2019, 47(5): 8.
- [6] 李 茜, 李 茹, 张 宇, 等. 低温等离子体协同催化处理甲苯废气的研究进展[J]. 当代化工, 2021, 50(3): 707-711.
- [7] Sungkwon J, Kimdae H. Effect of the electric conductivity of a catalyst on methane activation in a dielectric barrier discharge reactor[J]. Plasma Chemistry and Plasma Processing, 2014, 34: 175-186.
- [8] Zhu F S, Zhang H, Yan X, et al. Plasma-catalytic reforming of CO2-rich biogas over Ni/γ-Al2O3 catalysts in a rotating gliding arc reactor[J]. Fuel, 2017, 199: 430-437.
- [9] Mahammadunnisa S, Krushnamuty K, Subrahmanyam C. Catalytic nonthermal plasma assisted coprocessing of methane and nitrous oxide for methanol production[J]. Catalysis Today, 2015, 256: 102-107.
- [10] 方小杰, 赵 坤, 赵方利, 等. CeO2/LaFeO3用于甲烷化学链重整制取合成气反应性能研究[J]. 燃料化学学报, 2021, 49(9): 1250-1260.
- [11] 叶 凯, 刘香华, 姜 月, 等. 低温等离子体协同CeO2/13X催化降解甲苯[J]. 化工学报, 2021, 72(7): 3706-3715.
- [12] 徐 锋, 李 凡, 朱丽华, 等. Cu-Zn-Al基催化剂制备及催化等离子体转化甲烷制甲醇[J]. 高校化学工程学报, 2018, 32(4): 869-876.
- [13] 徐 锋, 于 淼, 李 凡, 等. 低温等离子体活化CH4-O2-N2-Ar-H2O体系制甲醇和合成气[J]. 黑龙江科技大学学报, 2021, 31(1): 21-27.
- [14] Magureanu M, Mandache N B, Eloy P, et al. Plasma-assisted catalysis for volatile organic compounds abatement[J]. Environ Sci Technol, 2005, 61(1/2): 12-20
- [15] 张 迎, 朱文杰, 张黎明, 等. CeO2中氧空位形成、表征及其作用机制研究进展[J]. 中国稀土学报, 2022, 40(1): 14-23.
- [16] 黄 亮. 非热等离子体促进甲烷活化转化的研究[D]. 杭州: 浙江大学, 2012.
- [17] Dow W P, Wang Y P, Huang T J. Effect of oxygen vacancy of support on copper oxide reduction[J]. J Catal, 1996, 160(2): 155-170.
- [18] Dow W P, Wang Y P, Huang T J.TPR and XRD studies of yttria doped ceriar alumina supported copper oxide catalyst[J]. Appl Catal A, 2000, 190(1/2): 25-34.
- [19] Bielanski A, Haber J. Oxygen in catalysis[M], New York: Marcel Dekker, 1991.
- [20] 陈 琳. 低温等离子体催化氧化甲烷合成甲醇的应用基础研究[D]. 杭州: 浙江大学, 2010.
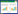 图 1 不同CuO与ZnO 物质的量比催化剂对甲烷转化率及产物产率的影响
Fig.1 Effect of different amount ratio of CuO and ZnO on methane conversion and product yield
图 1 不同CuO与ZnO 物质的量比催化剂对甲烷转化率及产物产率的影响
Fig.1 Effect of different amount ratio of CuO and ZnO on methane conversion and product yield